Selezionando l'opzione Sì, esci da Amgen.it comprendi che stai lasciando la pagina aziendale di Amgen italy e che verrai reindirizzato su un altro sito Internet appartenente a terzi, per i cui contenuti o opinioni Amgen Italy non è responsabile e non rilascia alcuna garanzia in merito a tale contenuto o alla sua accuratezza. Selezionando questa opzione e accedendo ai siti di terzi collegati, comprendi che lo fai a tuo rischio e pericolo.
Il sito web a cui verrai reindirizzato potrebbe essere progettato esclusivamente per i residenti di un particolare paese o paesi, come pubblicizzato su quel sito web. Di conseguenza, il sito web al quale verrai indirizzato potrebbe contenere informazioni su prodotti farmaceutici o indicazioni non approvate in Italy. Se risiedi in un Paese diverso da quello a cui è indirizzato tale sito web, contatta la tua affiliata Amgen locale per le informazioni corrette sui prodotti nel tuo Paese di residenza.
Nuova tappa del viaggio della ricerca Amgen alla scoperta di elementi inconsueti, spesso singolari, ma soprattutto importanti per la messa a punto di terapie innovative

In termini genetici, una cellula tumorale maligna può essere identica per il 99,999% a una cellula sana.
Quando gli illustratori medici raffigurano le cellule cancerose, di solito cercano di farle apparire spaventose e sinistre, come in questa immagine:
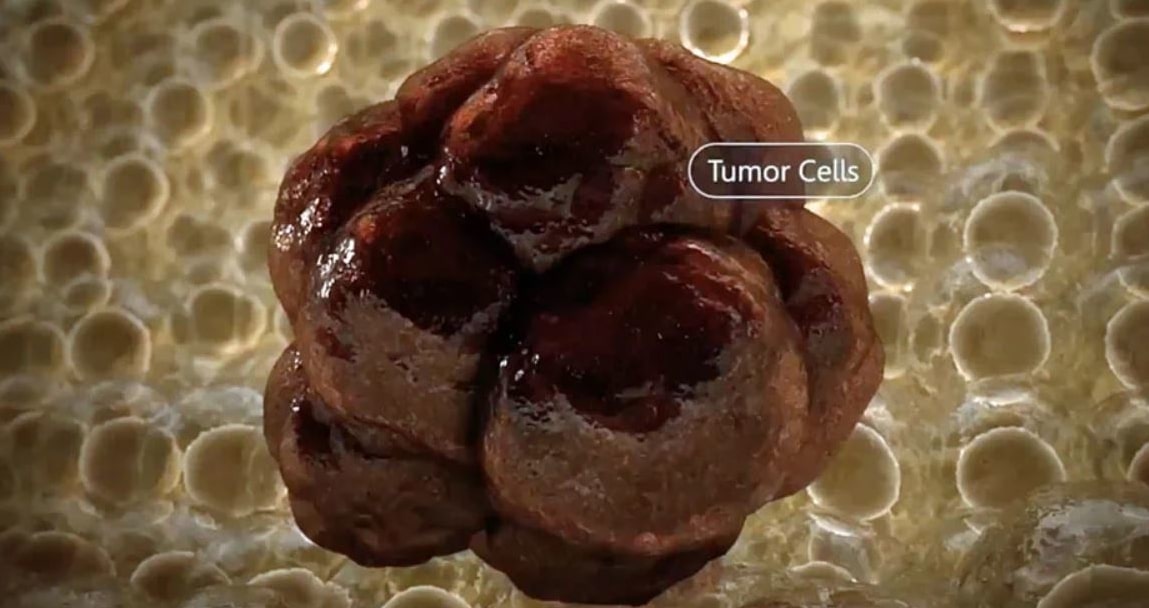
Purtroppo è difficile colpire in modo selettivo le cellule tumorali perché queste sono sorprendentemente simili a quelle sane, oggetto della loro minaccia. Se si confrontano i DNA di due persone non imparentate tra loro, in media ci sarà una differenza ogni 1.000. Ma se si confronta una cellula tumorale con una sana, prelevata dalla stessa persona, le differenze nel DNA potrebbero essere inferiori a un nucleotide ogni 100.000. Queste minuscole differenze possono però avere un grande impatto se interrompono i meccanismi proteici che regolano la normale crescita cellulare.
La somiglianza genetica tra cellule tumorali e normali rende difficile progettare farmaci ‘mirati’ che colpiscano efficacemente le prime ma lascino sostanzialmente illese quelle sane. È anche una delle ragioni per cui il sistema immunitario spesso non riesce a riconoscere e attaccare le cellule tumorali. Tuttavia il miglioramento dei metodi per il sequenziamento del DNA e del RNA stanno aiutando i ricercatori a individuare le sottili differenze delle cellule tumorali e a realizzare farmaci che colpiscano direttamente il cancro oppure attivino il sistema immunitario.
Il supercomputer più veloce impiegherebbe centinaia di anni per simulare i cambiamenti che avvengono in una proteina in un secondo.
Quando la biologia vuole fare qualcosa, assegna quasi sempre il lavoro a una proteina. Ecco perché quasi tutti i farmaci prodotti per curare la malattia sono ideati per legarsi a un bersaglio proteico e per modificare il comportamento della proteina stessa.
Negli articoli scientifici e nelle presentazioni, si vedono spesso immagini di proteine come questa:
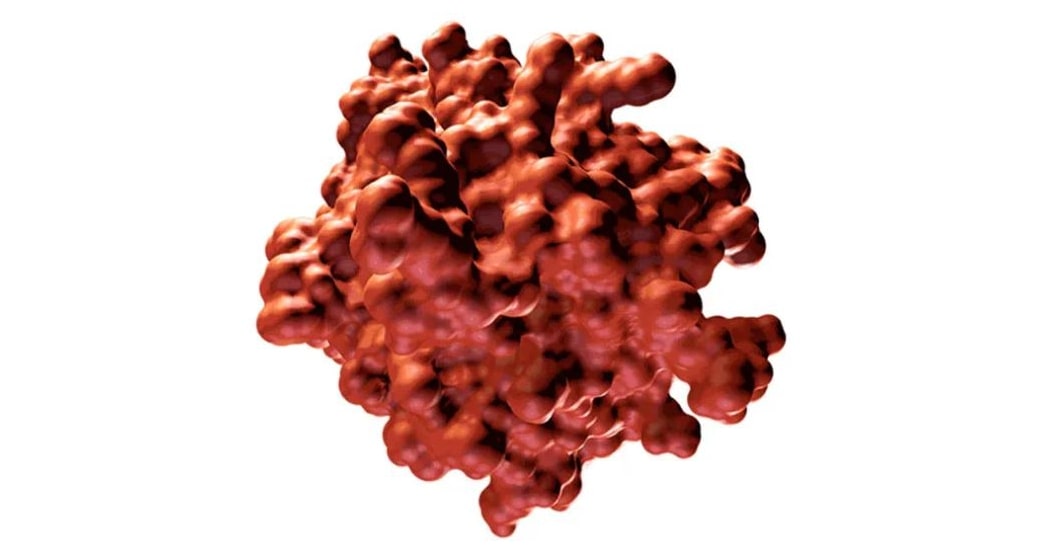
Quello che l’immagine purtroppo non può dire è che le proteine sanno essere incredibilmente dinamiche: non stanno ferme ma cambiano in continuazione la loro forma, talvolta in modo radicale, mentre gli atomi nella proteina interagiscono tra loro o con quelli nei dintorni. Il risultato è un vortice simile al cartone animato del diavolo della Tasmania, ma trilioni di volte più veloce.
A un supercomputer convenzionale servirebbero mesi solo per calcolare pochi milionesimi di secondo del comportamento e delle interazioni delle proteine. I sistemi più recenti, progettati specificamente per simulare la dinamica molecolare, sono in grado di svolgere lo stesso lavoro molto più velocemente, ma hanno ancora molti limiti nella durata delle simulazioni che possono eseguire in un lasso di tempo ragionevole. Anche se ora possono fare ‘solo’ in giorni ciò che prima richiedeva mesi, ancora oggi il più veloce di questi computer dedicati impiegherebbe centinaia di anni per simulare un secondo di comportamento delle proteine.
Fortunatamente, anche questa scala temporale ci consente ancora di imparare molto. In alcuni casi, le simulazioni hanno rivelato che le proteine che sembrano non somministrabili nella loro forma più comune possono assumere rapidamente altre forme, tali da permettere alle molecole dei farmaci di penetrare le loro difese.
Le persone affette da una malattia genetica chiamata sclerosteosi possono avere ossa praticamente indistruttibili, anche in caso di incidenti gravi, come quello con una motocicletta contro un albero!
La sclerosteosi è una condizione molto rara causata dalla mancanza di un gene funzionante per una proteina chiamata sclerostina. Questa proteina funziona come un interruttore per le cellule dell’apparato scheletrico e, senza di essa, il corpo continua a costruire tessuto osseo, fino a che le ossa raggiungono un’elevatissima densità. È noto che coloro che vivono questa rara condizione superano senza alcuna frattura incidenti anche molto seri, come quelli in auto e moto, oppure cadute gravi. Ma, nel tempo, la sclerosteosi causa anche seri problemi, poiché la crescita ossea eccessiva incide gradualmente su altre funzioni biologiche critiche.
Condizioni genetiche rare come la sclerosteosi o l’ipercolesterolemia familiare (livelli anomali di colesterolo LDL) possono aiutare a far luce su forme più comuni di malattia rivelando i geni e le proteine che svolgono un ruolo importante nella normale biologia. I farmaci che prendono di mira le proteine chiave, identificate attraverso mutazioni genetiche, possono aiutare a modulare la biologia in modi che trattino le malattie e migliorino la salute.